PUBLICIDADE
Os álcoois podem sofrer oxidação quando expostos a algum agente oxidante, como uma solução aquosa de dicromato de potássio (K2Cr2O7) ou de permanganato de potássio (KMnO4) em meio ácido.
Um oxigênio nascente [O] que estiver no meio irá atacar o carbono ligado ao grupo funcional do álcool (hidroxila – OH), formando um composto muito instável, chamado de diol gêmino, que possui duas hidroxilas ligadas a um mesmo carbono. Por ser instável, esse composto libera água e dá origem a um novo produto.
Esse produto irá depender do tipo de álcool que foi oxidado, se é primário, secundário, terciário ou se é o metanol.
Resumidamente, temos:
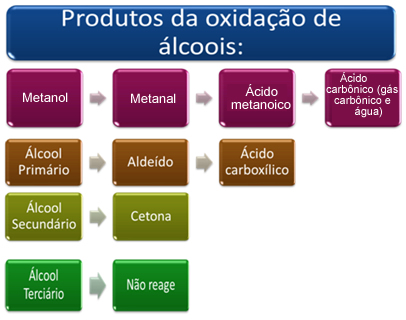
Veja cada caso a seguir:
- Metanol (H3C─ OH):
O metanol é o único álcool que possui três hidrogênios ligados ao carbono que sofrerá a oxidação. Nesse caso, visto que há três pontos na molécula que um oxigênio nascente pode atacar, ocorrerão três oxidações sucessivas, como mostrado no esquema abaixo:
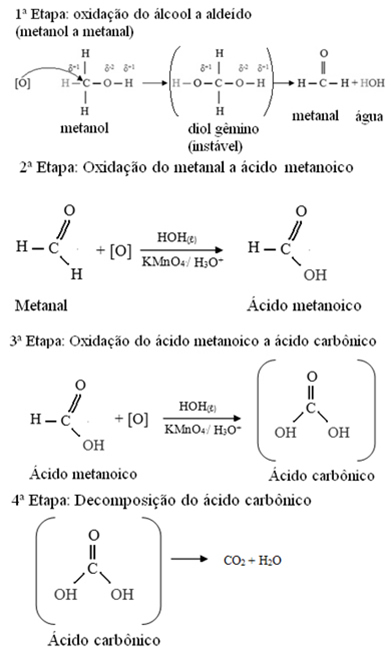
- Álcoois primários:
Nesses compostos, o carbono da hidroxila está ligado a apenas um átomo de carbono, ou seja, os dois outros ligantes são hidrogênios, havendo dois lugares para o oxigênio nascente atacar.
Primeiramente, haverá a formação de um aldeído, como mostrado a seguir:
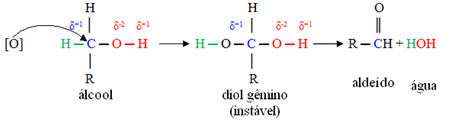
Mas, a oxidação continua, porque os reagentes utilizados para oxidar o álcool são mais fortes do que os usados para oxidar um aldeído. Então, outro oxigênio nascente ataca o carbono da carbonila e produz um ácido carboxílico.
A seguir, temos um exemplo, a oxidação do etanol, primeiramente a etanal e depois a ácido etanoico (ácido acético). Essa reação total é a transformação do vinho em vinagre.
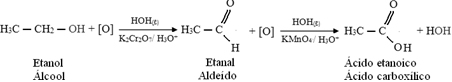
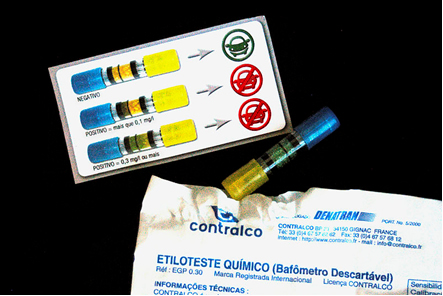
A oxidação parcial do etanol a etanal é a que ocorre quando uma pessoa alcoolizada faz o teste de bafômetro descartável. Dentro desse aparelho há uma mistura sólida de dicromato de potássio e sílica em meio ácido, ocorrendo a seguinte reação:
K2Cr2O7(aq) + 4H2SO4(aq) + 3 CH3CH2OH(g) → Cr2(SO4)3(aq) + 7H2O(l) + 3 CH3CHO(g) + K2SO4(aq)
Alaranjado etanol (incolor) verde etanal (incolor)
Veja que, além da oxidação do etanol (álcool) a etanal (aldeído), ocorre simultaneamente a redução do dicromato, que é alaranjado, a cromo (III), ou mesmo a cromo (II), que é verde. A mudança da cor indicará que a pessoa está com álcool no sangue acima do permitido.
- Álcoois secundários:
Esses são compostos em que o carbono da hidroxila está ligado a dois outros átomos de carbono e a apenas um átomo de hidrogênio. Portanto, só haverá uma localização na molécula em que o oxigênio nascente poderá atacar e será formado apenas um tipo de produto, que sempre será uma cetona:
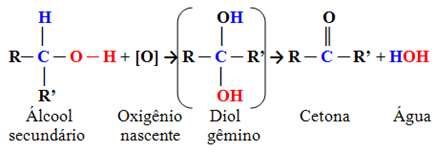
Visto que o carbono da carbonila de uma cetona não possui nenhum hidrogênio ligado diretamente a ele, não haverá mais possibilidade de continuar a oxidação. Por isso, a reação para na cetona.
- Álcoois terciários:
Os álcoois terciários são aqueles em que o carbono que possui o grupo – OH faz três ligações com outros átomos de carbono. Como eles não fazem ligações com hidrogênios, não há nenhum ponto na molécula que possa ser atacado por um oxigênio nascente. Devido a esse fato, os álcoois terciários não sofrem oxidação.
* Fonte e autor da imagem: CostaPPPR.
Por Jennifer Fogaça
Graduada em Química