PUBLICIDADE
Em 1874, o químico holandês Jacobus Henrique van’t Hoff (1852-1911) e o químico francês Joseph Achille le Bel (1847-1930), por meio de teorias matemáticas, sugeriram de modo independente a existência de carbonos assimétricos.
Na época, eles foram criticados duramente, principalmente van’t Hoff, pelo famoso químico alemão Adolph Wilhelm Kolbe (1818-1884). No entanto, Kolbe estava enganado, hoje sabemos que existe sim um carbono assimétrico, tanto que, em 1901, van’t Hoff foi o primeiro químico a receber o prêmio Nobel.
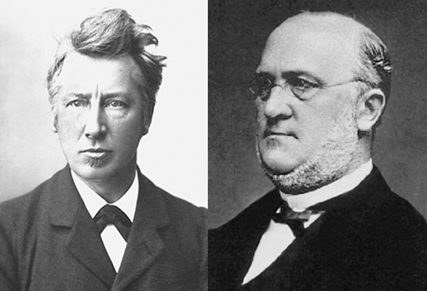
van’t Hoff (à esquerda) e Kolbe (à direita)
Uma das condições necessárias para que a molécula possua atividade óptica é que ela seja assimétrica. Além disso, um modo de verificar se ela é assimétrica é estudando sua estrutura detalhadamente para ver se ela possui, pelo menos, um carbono assimétrico.
O que é uma molécula assimétrica e um carbono assimétrico?
Algo simétrico é aquilo que possui pelo menos um plano de simetria. Por exemplo, se cortarmos uma raquete de tênis ao meio, as duas partes resultantes serão exatamente iguais. Além disso, se as colocarmos de frente a um espelho plano, irão produzir uma imagem idêntica.
Já as estruturas que não admitem plano de simetria são denominadas assimétricas. Um exemplo é a nossa mão, pois se a colocarmos diante de um espelho, ela produzirá uma imagem diferente dela própria. Se colocarmos a mão direita, a imagem será a da mão esquerda e vice-versa. Outro ponto importante é que elas não são sobreponíveis.
É por isso que o carbono assimétrico também é chamado de carbono quiral, sendo que essa palavra origina-se de khéir que em grego significa mão.
Um exemplo de molécula assimétrica é a talidomida, cuja estrutura é mostrada a seguir:
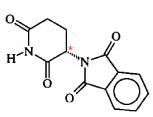
O ponto localizado com um asterisco (*) corresponde a um carbono assimétrico, pois ele possui quatro ligações covalentes que são feitas com diferentes átomos ou grupos de átomos.
Abaixo temos um carbono com quatro ligantes diferentes na frente de um espelho. Observe que a imagem não pode ser sobreposta sobre a estrutura original:
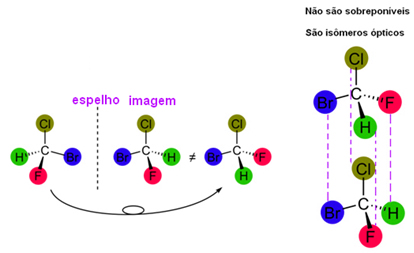
As duas moléculas obtidas acima são isômeros ópticos ou enantiômeros.
Voltando ao caso da talidomida, devido ao fato dela possuir carbono assimétrico, o resultado é que a molécula passa a ter uma imagem não superponível, o que corresponde à outra substância. Assim, temos dois isômeros da talidomida com propriedades extremamente diferentes.
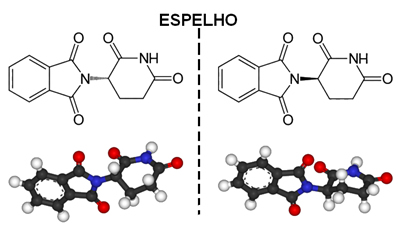
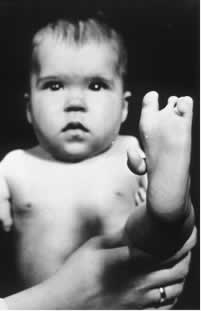
Um desses isômeros (R) possui propriedades sedativas. Por isso, no final da década de 50, ele passou a ser usado como medicamento tranquilizante e sonífero para grávidas. Isso desencadeou uma tragédia, pois o seu enantiômeros (S) também estava misturado ao medicamento. Esse isômero, por sua vez, é teratogênico e levou várias gestantes a terem seus bebês com mãos, pernas, braços e pés atrofiados.
Por Jennifer Fogaça
Graduada em Química